与生物膜作斗争
J. W. Costerton,(蒙大拿州立大学生物膜工程中心主任)
Philip S.Stewart,(蒙大拿州立大学生物膜工程中心副主任)
目前,五角大楼的策划者们十分重视信息战。原因何在?因为干扰敌人的信息交流能力比摧毁其军事工事或工厂的威力大得多。在与有害细菌的斗争中,有些研究者正在考虑相同的战略。

许多引起顽固性感染的细菌把它们自己组织成复杂坚韧的薄膜——生物膜,它们几乎不可能被常规的抗菌素清除。过去几年间医学研究者已发现,生物膜中的细菌严重依赖相互之间的信号传导能力,能干扰其传导的药物可能阻挡这些细菌引起感染或彻底摧毁它们的坚固防线。这类药物可能用以对抗形形色色的疾病,诸如反复折磨囊性纤维化患者的肺炎以及医学移植物周围的缓慢发作的感染。
目前,正在动物实验中评价信号阻断化合物。为什么时至今日才准备把这些精良的武器纳入医学武器库呢?一言以蔽之,原因是,微生物学家花了很长的时间来摸清敌人的底细。19世纪晚期德国的Robert Koch实验室证实了疾病的微生物起源说。从此,包括科学家在内的大多数人都视细菌为单细胞,它们在某些水样环境中或体液内漫游。研究者们存研究这些微生物时通常将显微镜对准悬浮在水滴中的培养细菌。该方法方便但井不完全合适,因为这些实验条件不能反映微生物的实际环境。因此,在标准实验室培养的细菌与自然界中的细菌根本不一样。
近年来,我们与其他细菌学家对常见病原微生物到底如何生活的认识获得了重大进展。我们的研究显示:实际上,许多微生物以单个细胞形式飘浮的时间并不长,相反,它们以有组织的集落粘附在各种湿润表面,从而形成惊人多样化的群体。
回顾过去,令人惊讶的是,研究人员竟然如此长时间地忽视了微生物的这种生活方式。毕竟,细菌的生物膜是普遍存在的——大多数人每天都会遇到的牙斑、小溪石头上的滑膜、2-3天后花瓶内面不可避免地要长出的粘滑物都是常见的实例。我们研究的焦点不仅仅是细菌制造生物膜的能力。事实上,微生物的遗传多样性可将它们自己排列成活的装饰板及其它们侵犯的宽广环境,这使我们相信这种能力一定是细菌生长的古老策略。然而,现代才对此策略进行科学评价和了解。
平地上的细菌
事实上,一些生物学家早就尝试用普通显徽镜甚至用电子显微镜观寮在生物膜中生长的细菌。他们总是看到一些细菌,但没能获得深层生长的清晰图像。他们由此认为这些内部细菌大多数已经死亡并形成杂乱无序的凝块。大约十年前这种观点才发生改变,当时细菌学家开始应用激光扫描共焦显微镜技术。这种技术使研究者们能对活的生物膜进行不同深度的分层现察,并将这些平面合成三维结构。1991年,加拿大国立水研究所的John R. Lawrence与萨斯喀彻温大学的Douglas E. Caldwell以及Costerton在一个研究生物膜结构的合作项目中应用上述方法首次发现细菌生长在一小块土地,我们称之为微小集落(microcolony)。细菌所占不到三分之一,其余都是细菌分泌的粘性物质,它们吸收水分并网住小分子。

这些粘性物质,或更正规地说细胞外基质,将各个微小集落拉在一起。一个生物膜由无数个这种小团体组成,由网状的开放水道隔开。流经这些小管道的液体浸泡着细菌集落,为它们提供溶解的营养物,并移去废物。位于微小集落以外的细菌受到这一管道系统的良好供应,但对其内部的细菌,此管道系统大多数被切断围绕着它们的密集的细菌及将它们粘在一起的有机基质共同形成水流的屏障,所以在集落内的细菌必须制造营养物,而不是靠扩散给它们。实际上其供应并不都是那么贫乏,因为这些粘性物质大多数都只是水分,小分子可在其中自由通过,虽有某些重要的例外。假如有些物质在途中与细菌或基质相互作用,则难以扩散到微小集落的中心。
这种化学反应在细菌微膜内产生小范围的环境改变。在利用共焦显微镜阐明其原因之前,已经发现这些改变。1985年我们的同事Zbigniew Lewandowski开始用尖端直径仅0.01毫米的针形微电极直接测量其化学组成。他的发现之一是,其氧浓度差别很大,即使其位置相距仅0.05毫米,即比人的头发略大。科学家们常观察细菌中的氧量,因为它可以反映细菌的生理状态。例如,由铜绿假单胞菌(该菌可引起囊性纤维化肺炎)组成的生物微膜,只有氧气能透入到的地方即每一菌落之外0.02-0.03毫米处,细菌才有活性并生长。再深入一些,细菌是活的但在休眠状态。这种代谢状态的多样性与在实验室培养中见到的均一性具有明显的区别。
单一生物膜内化学环境的差异意味着一个细菌可能与另一细菌在形态与功能上有很大差别,即使两个细菌在遗传上是相同的。同样,局部条件控制生物微膜内的细菌产生多种毒素及其他致病物质,结果,有些细菌对宿主毫无危害,而另一些细菌对宿主可能是致命的。条件的巨大差别可能使几种细菌共同生活与繁殖。有时,一种细菌靠另一种细菌的代谢产物来养活,对二者都有利。
自20世纪40年代以来,已经知道一件有趣的事:牛或其他反刍动物吃了饲料后,生物微膜就形成在饲料上。这些微膜原来是有消化植物中的纤维素并产生脂肪酸的细菌组成的。当这些吃纤维素的细菌产生了足够的脂肪酸以抑制其自身生长时,移动的螺旋菌与其他细菌侵入生物微膜,并用此来进行其自身代谢。这些饲料逐渐消失,变成一团细菌,以后被动物所消化。所以牛靠生物微膜生活而不是稻草。
对反刍动物而言,这些微膜是不可缺少的,但对我们人类而言,它们是危害,有时甚至是对人类健康的严重威胁。它们能在大多数医学或工业上采用的杀菌处理中存活。这些处理可以迅速去除自由漂浮的细菌。他们能够躲开免疫系统释放的分子与细胞。因此,生物微膜感染往往十分持久。
坚韧的虫子
为什么这些生物膜如此有活力呢?有时,抗生素与抗菌清洁剂不能穿过生物膜。例如青霉素很难透过含有产生β-内酰胺酶的细胞的生物微膜。这些酶在抗生素透进生物膜之前就把它降解了,因而抗生素无法达刊微膜的深层。即使是家庭或工业上常用的漂白粉亦很难去除生物微膜.这一氧化剂最后能进人内部,但必须逐层克服微膜的中和能力。这一过程需要的时间比想像更长。因此,人们很容易误认为全部细菌已死完,但实际上许多细菌仍然活着。
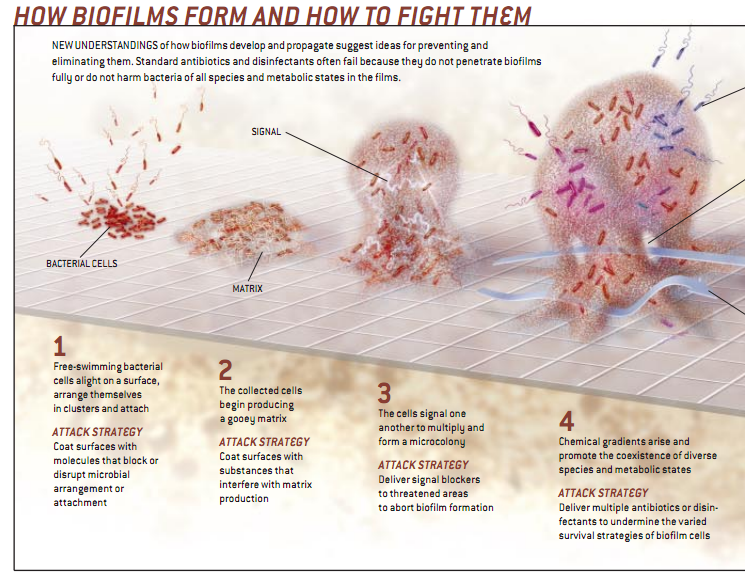
尚有其它因素增强其顽固性即使是抗菌物质很容易地透过生物微膜,细菌仍然活着,而自由漂浮的细菌早已杀死。这一能力长期迷惑着生物学家,但最近他们知道生物微膜中的各种情况与不同的细菌类型赋予了生物膜对抗抗菌药的本领。
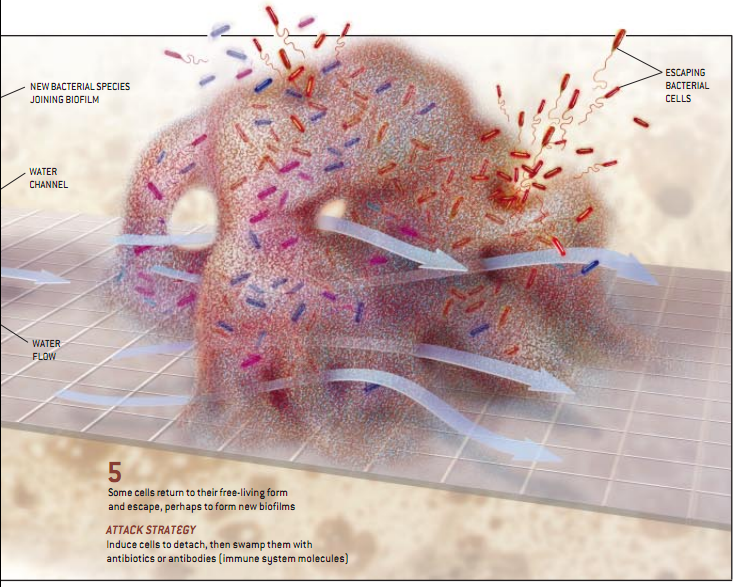
再举青霉素为例,它能攻击多种细菌细胞的复制。若生物微膜中存在缺乏某种主要营养的区域,这些区域的细菌虽然存活但不复制,就将暴露给青霉素。由于活跃与不活跃的细菌在生物微膜中混合存在,而且残存的细菌能利用死的细菌作为营养,在抗生素治疗后幸存的细菌在几小时内就能恢复它们原来的微膜。
这种能力可以解释在培养细胞中效果很好的抗菌剂为什么不能帮助人们有效地与生物微膜作斗争。这些人大多数是医生和患者,但还有许多人是工程师,他们必须与破坏机器或腐蚀金属管道的工业生物微膜作斗争。为了帮助他们,1990年国家科学基金会在蒙大拿州立大学建立了工程研究中心(现在成为生物膜工程中心)。我们俩已在此合作了10年。
该中心的研究发现,当细菌粘附在表面并形成生物微膜时,它们制造了数以百计的在自由漂浮的细菌中没有见到的蛋白质。正如哈佛大学医学院Roberto Kolter与其同事通过去除多种细菌的某些基因(蛋白质的蓝本)的方法所揭示的那样,其中某些蛋白质与细菌从接触表面到固定位置前的奇怪滑动有关。用引起常见的葡萄球菌感染的表皮葡萄球菌(Staphylococcus epidermidis),其它研究者发现了控制生物微膜形成的下一个步骤(细胞外基质合成)的基因。当这些基因被灭活时,细菌丧失其在试管中形成生物微膜的能力,显然同样情况可发生在实验动物的组织中。
近年的实验显示在其它微生物中有相似的遗传控制中心。例如,铜绿假单孢菌含有几种基因,当该细菌接触到表面时,15分钟内这些基因就开启了。其中一种基因algC乃合成藻酸盐所必需。藻酸盐是形成细胞外基质的胶样多聚物。
聚集到一起来形成生物膜的细菌如何首先知道联通某些基因呢?答案是这些看上去简单的孤立细菌经常相互通讯。就铜绿假单胞菌和一大组相似的细菌而言,其相关的信号分子是酰化高丝氨酸内酯,每个细胞产生该物质的量笑浓度上升,继而启动十余个基因。宾厄姆顿大学的David G.Davies已经揭示了这种机制,他称之为法定人数意识(quorumsensing),是生物膜发育的关键。事实上,铜绿假单胞菌缺失该基因后,不能形成生物微膜,而只是形成无序的堆砌。
研究者们发现了生长在导尿管中的生物微膜的信号分子这类微膜及永久性医学移植物中的微膜引起最为头痛的生物微膜感染,在美国每年约有1000万人受累。虽然它们发展很缓慢,但是这缓慢发展的感染常常反复复发,极难根治。生物微膜亦与牙周疾病、前列腺感染、肾结石、结核、军团病及一些中耳感染有关。
现任生物学家们了解了生物微膜是如何形成的,用针对其特性的药物来控制它们已成为可能例如可以用一种分子来削平细菌表面的粘性物质,从开始就减少其粘附表面并形成薄膜的能力,另一种选择是干扰其细胞外基质的合成,如在医学移植物上溶一层化学物质以排除产生基质的基因也可以作用于生物微膜分子中细菌用以交换信息的分子,以阻止生物微膜的形成或抑制其毒素产生或抑制其它同样有害的作用。也就是,不用毒素去杀伤细菌,科学家们将用一种更巧妙的方法对细菌的损害作用进行阻断。
对抗生物膜的战术
事实上,在商业上已至少开始开发一种新药。1995年,澳大利亚悉尼新南威尔士大学的Staffan Kjelleberg与Peter Steinberg指出,在植物学湾的一种红藻(Deliseaputchra)的叶上很少发现有生物微膜。虽然在该水域中有几千株细菌在旺盛地生长,但是藻类标本上却没有斑点。这是怎么回事?Kjelleberg与Steinberg确定.红藻利用呋喃衍生物使它沾不上生物微膜。这些研究者与其大学现在组建了一个公司(Biosigna1)来生产含有呋喃衍生物的保护膜,用于船壳和水产养殖设备。

过去几年间,研究者们对Kjelleberg与Steinberg分离的呋喃衍生物的作用机制有了更深刻的认识这些物质类似两类细菌分子:一类是许多制造生物微膜的细菌用的酰化高丝氨酸内酯另类是普林斯顿大学Bonnie L. Bassler所描述的分子,几乎所有细菌都用它来在不同种属细菌间传递信息。显然,呋喃衍生物可结合到细菌的本来该由其它信号结合的地方,从而阻止信号分子传递促进生物微膜形成的信号。标志就是,呋喃衍生物既可防止生物微膜形成,亦可破坏已有的生物微膜在医疗中的应用亦比较理想,因为它们无毒,在体内比较稳定而且呋喃类在海洋中已存在数百万年,没有引起细菌的抗性,因而有希望在应用时不发生抗药性。

这一研究路线亦提供了一个目前尚少实用意义、但可能最终证明同样重要的问题,它使人们对细菌的概念发生了革命性的变化。生物学家借用平常描述胚胎生长的语言,现在开始叙述生物微膜的形成犹如一个发育过程正如受精卵在胚胎发育中产生了不同的细胞,细菌亦可以在接触到表面后进行分化。它们合成信息传递分子,类似昆虫或动物的信息素或激素,共同建筑结构精细的微菌落。该设计使营养进来废物运出,类似高等生物的循环系统。在一些生物微膜中,多种细菌合作共同完成一种细菌难以完成的消化。这些观察结果提示许多生物学家长期认为是低等的细菌可能在生命系统中处于以往不曾想象过的较高等级。
导尿管中的麻烦
在导尿管中形成的生物微膜是常见的感染源。导尿管留量时间很短时,没有什么危险,但危险性随留置时间延长而增长。例如1996年的研究发现导尿管留置1周,有10-50%患者发生感染,留置1月,全部患者发生感染。
特洛伊木马
尽管十分注意,有时生物微膜的细菌还是进入了生物医学产品。在1993年与1994年100名哮喘患者死去了,因为在他们使用的albutermol吸入剂中含有能形成生物微膜的铜绿假单孢菌。其来源可追踪到制造该药的一个容器。1989年另一个著名的生物微膜细菌P.cepacia在一个装强力防腐剂(povidone碘液)的瓶子中聚集,引起德克萨斯州一家儿童医院患儿感染。
腐蚀的原因
有些生物微膜在工业中引起严重的麻烦,因为它们可以在金属管道内长成菌落,加速管道腐蚀,是火电厂强修的一半原因。公司将每年花费数十亿美元来解决这一问题。
水的污染
饮用水源亦可被生物微膜所污染。它常常生长在配水管内部,致病菌在一层黏性物质的保护下,能抵抗漂白粉而繁殖。斯坦福大学研究者们发现引起霍乱的霍乱弧菌能耐受常规用于消毒水的氯浓度的10-20倍。1996年生物微膜反复引起华盛顿特区的水源在细菌含量上违反联邦政府的标准。
【范维珂/译冉隆华/校】
请 登录 发表评论