撰文/Carol Ezzell
(原文:Hope In A Vial,pp28-35.June 2002)
1984年,当引起艾滋病的HIV病毒首次被发现时,人类并没有意识到艾滋病疫苗的研制过程有多么艰难。美国卫生部的秘书MargaretM.Heckler当时预测,两年内就可研制出有效的疫苗,使人们免受艾滋病的折磨。现在看来,这种估计是不是有些草率?
在过去大约20年里,艾滋病肆意流行,仅去年全球就有4千万人感染了HIV病毒,300万人死于艾滋病(其中北美洲2万人)。尽管被研究人员看好的几种艾滋病疫苗正在进行临床试验,但迄今为止还没有一种达到了预期的目标。初试的结果让研究人员满怀希望,然而最终的结局却是以一次又一次的失败告终。两年前,甚至有艾滋病研究人员私下表示,不知是否能够在有生之年研制出具有一定防治性的艾滋病疫苗。尽管艾滋病研究一直没有令人吃惊的突破,但是一些鼓舞人心的数据让已经疲惫不堪的艾滋病疫苗研究者看到了一丝希望。研究人员在黑暗中摸索了10多年,尽管屡次受挫但他们并不气馁,正准备从新的方向开辟道路。纽约男同性恋健康危机组织治疗与预防主任Gregg Gonsalves说:“当前的艾滋病研究进入了一个有趣的阶段,就像是戏剧的第二幕刚刚开始。”
在戏剧中,第一幕介绍人物和背景;第二幕矛盾深化,真正的斗争开始上演。在艾滋病疫苗的研制过程中,第一幕就是发现可以导致严重疾病的病毒之一——HIV病毒(起初被称为逆转录病毒)。与其他病毒不同的是,逆转录病毒(retrovirus)可以让自身遗传因子巧妙地进入到受病毒入侵的体细胞中,使病毒基因在被感染的细胞中永久存在,并遗传给子代细胞。逆转录病毒复制的速度可快可慢,发生突变的几率非常大,这使得HIV病毒可以改变外型,从而导致机体的免疫系统和抗逆转录病毒的药物失去作用。
在第一幕中同时登场的还有HIV病毒的敌手——机体的免疫系统。该系统是由抗体(一种可以黏附和标记出类似病毒的Y形分子)和细胞毒性或杀伤性T细胞组成(一种白细胞,可以破坏被病毒感染的细胞)。在被感染后的几年,机体的免疫系统和HIV病毒展开激烈的斗争,每天数百万的新生杀伤性T细胞会与数亿个来自被感染细胞的病毒作战。另外,免疫系统在病毒感染的早期,会产生大量HIV抗体,尽管抗体对于这个特殊的敌手并不是非常有效。
当第二幕开场时,HIV病毒仍然活跃在舞台上。首次大规模艾滋病疫苗试验的结果将于今年年底产生,但几乎没有科学家对其持乐观态度,因为此前的分析表明该疫苗效果非常微弱。同时,另一项由美国资助的艾滋病疫苗试验计划于今年九月在泰国进行,目前也引起了各方的争议。但无论如何,研制疫苗仍需要通过各种方法来引起艾滋病研究组织的高度重视。目前出台的各种方案也引发了关于艾滋病疫苗研究的大讨论:究竟是能够诱导出完全保护机体免受HIV病毒感染的免疫反应疫苗有用,还是比这个标准稍微低一些的疫苗有用?一些科学家意识到,那些可以诱导产生免疫反应的疫苗具有潜在的价值,这种免疫反应可以在细胞遭受病毒感染的早期就将病毒消灭。科学家认为,这种疫苗可以更有效地限制病毒的繁殖而非增强机体的自然反应,从而帮助HIV感染者延长寿命,并延缓艾滋病的发病期。
20世纪90年代初,科学家认为,通过对无症状艾滋病病毒携带者(即感染HIV病毒10年以上尚无任何症状的患者)的长期研究,可以研制出最好的艾滋病疫苗。然而不幸的是,许多长期无症状携带者最终还是逃不出病毒扩散的厄运。美国康奈尔大学Weill医学院的John P.Moore说:“这些人相对长寿的原因可能是由于病毒自身感染力较弱或是机体有较强的免疫力。”换句话说,就是这些人非常幸运,感染上了扩散比较缓慢的HIV病毒,机体的免疫系统正好可以将它们围困在其中,使之无法扩散。
自然界存在其他免疫反应吗?
艾滋病疫苗的研制者奋斗了几十年,一直在寻找HIV的“相关免疫反应”(几种免疫的复合反应)。这种复合反应一旦被疫苗所诱导,将会保护机体免受感染。然而,研究者还是空手而归,因为他们无从下手来寻找这种艾滋病疫苗。哈佛大学公众健康学院的Max Essex承认:“我们正在试图诱导一种在自然界尚未发现的免疫反应”。艾滋病疫苗的研究工作看上去有些漫无目的。
要证明一种艾滋病疫苗是否有效,就必须经过三个阶段的临床试验。第一阶段的试验需要给数十名志愿者注射疫苗,确定疫苗对人体是否有害以及适用的剂量;第二阶段试验在上百人的群体中进行,以观察疫苗诱导免疫反应的能力;第三阶段的试验是给数千名志愿者注射疫苗,并长期随访,确定他们是否免受感染。不论使用何种药品,这三个阶段试验所需的费用都非常昂贵,并且很难得到主管部门的批准。然而,艾滋病的试验更具有挑战性,原因在于一个具有讽刺意味的需要:注射疫苗的受试者必须听取研究人员所叮嘱的如何降低感染机率的建议,例如:要使用避孕套;对于吸毒的人来说,要使用干净的针头,因为HIV病毒是通过性和血液接触的方式传播的。然而疫苗试验要取得预期的效果,就必须在受试者没有听取咨询意见、不采取任何防范措施的情况下进行。
第一种达到三个阶段试验标准的艾滋病疫苗是由gP120组成。gP120是HIV病毒胞膜上的一个蛋白分子,HIV可以通过它黏附到细胞表面并使之感染。理论上讲,血液中存在的gpl20可以刺激机体的免疫系统,使其在抗体受到HIV病毒感染时,迅速对HIV病毒表面的gpl20进行攻击。
这种疫苗是位于加州布里斯班的VaxGen公司(该公司是位于南旧金山的生物技术公司Genentech的子公司)研制的。研究人员在北美和欧洲的5400多名患者(多数为同性恋者)、南亚的2500名静脉注射吸毒者身上使用了这种疫苗;1998年在北美和欧洲的试验结果有望在今年年底产生。
许多艾滋病疫苗研究人员对VaxGen公司的试验表示怀疑,因为病毒表面的gpl20通常以三聚体的形式存在,而VaxGen公司研制的疫苗只使用了gpl20的单分子形式,而且这种由蛋白分子组成的疫苗只能刺激机体产生抗体一种体液免疫反应,而不能刺激机体产生包括细胞毒性T细胞在内的细胞免疫。越来越多的研究人员认为,要预防艾滋病只依赖单独的抗体反应是不够的,还需要强大的细胞免疫反应。
事实上,早期的研究结果并不令人鼓舞。去年10月,一个独立的数据审查小组对北美和欧洲的试验数据进行了分析。尽管该小组经过分析认为,这种疫苗对志愿者没有任何毒副作用,一旦疫苗有任何反应,评委们有权建议停止试验。但试验并没有停止。
VaxGen公司声称,他们将争取美国食品和药品管理局(FDA)批准,同意该疫苗上市,虽然三个阶段的试验结果显示该疫苗只能使人体感染病毒的几率下降30%。公司总裁和合作伙伴Donald P.Francis称,1954年JonasSalk研制的脊髓灰质炎疫苗(polio vaccine)只有60%的有效率,却使美国脊髓灰质炎发病率迅速而戏剧般地降低了许多。
如果有人只接受了部分有效的艾滋病疫苗注射就麻痹大意,以为自己已经受到保护,可以任意参与那些易引起病毒发作的危险活动,结果反而会产生副作用。哈佛大学公众健康学院的KarenM.Kuntz和Elizabeth Bogard已经构建出计算机模型,模拟这种疫苗在泰国吸毒者身上注射后的效应。根据计算机模型显示,如果90%已接受疫苗的人重新共用针头或使用不卫生的针头,使用有效率为30%的疫苗并不会降低艾滋病在人群中的传播速度;如果疫苗的有效率至少达到75%,这种反复的吸毒行为才可能不会危害到公众的健康。
计划在泰国进行的一项约有1. 6万人参加的研究也是三个阶段的大规模试验,同样也引起了争议。该疫苗将VaxGen公司的疫苗和金丝雀痘病毒(canarypox virus)重组,这种金丝雀痘病毒内已经被科学家注入了编码gpl20fD另外两种蛋白(其中一种蛋白参与构成HIV病毒的核心,另一种可以使病毒复制)的基因。这种经过基因工程改造后的金丝雀痘病毒可以进入细胞内,并将HIV的碎片在细胞表面展现出来,从而刺激免疫系统。
围绕gpl20/金丝雀痘病毒疫苗的科学价值而展开的政治争论和质疑延缓了对该疫苗进行的广泛试验。起初,美国国家过敏性与感染性疾病研究所(NIAID)和美国国防部计划同时重复该试验,但是NIAID在研究第二阶段的试验数据时,发现只有不到30%的志愿者可以产生抵抗HIV的细胞毒性T细胞,于是他们放弃了这项研究。经过官方的协商,今年1月白宫将拨给国防部的试验经费转给了NIAID,作为支持艾滋病研究的部分努力。NIAID的艾滋病疫苗研究组的助理主任PeggyJohnston说,她期待进行一项艾滋病疫苗的试验。同时她也强调:“这次试验是在泰国进行的,我们不希望有任何人(NIAID成员)受到影响。”
评论家认为,这些政治上的伎俩正阻止着艾滋病的研究。一个怀疑论者说:“在试验中很少有科学的东西介入其中。”他还想知道为什么泰国人不提出质疑:“如果不能对美国有利,又怎么会对我们有利?”其他人认为,由于该试验是由国防部主持的,因此试验结果只能证明这种疫苗是否有效,他们不会收集数据让科学家分析其潜在的失败原因。
局部保护作用
在这幕戏中默克(Merck)公司登场了,该公司同时在完成两种不同的待测疫苗的第一阶段试验。今年2月,在西雅图第九届逆转录病毒和机会感染会议上,默克公司从事艾滋病疫苗研究的资深副总裁Emilio A.Emini将两种疫苗试验的初始数据公布于众,让在场的科学家惊叹不已。
第一个试验是研究由HIV病毒的gag基因(此基因编码了HIV病毒的核心置臼)构成的疫苗,该疫苗被称为裸DNA疫苗(naked DNA vaccine),完全由DNA构成。细胞可以摄取gag基因,并以它为模板合成病毒蛋臼,进而依次诱导较弱的(也可能是无用的)体液免疫反应和较强的细胞免疫反应(见60页图示)。Emini和同事指出,42%的志愿者注射了最大剂量的DNA疫苗后,体内会产生更多的能够杀伤HIV病毒的T细胞。
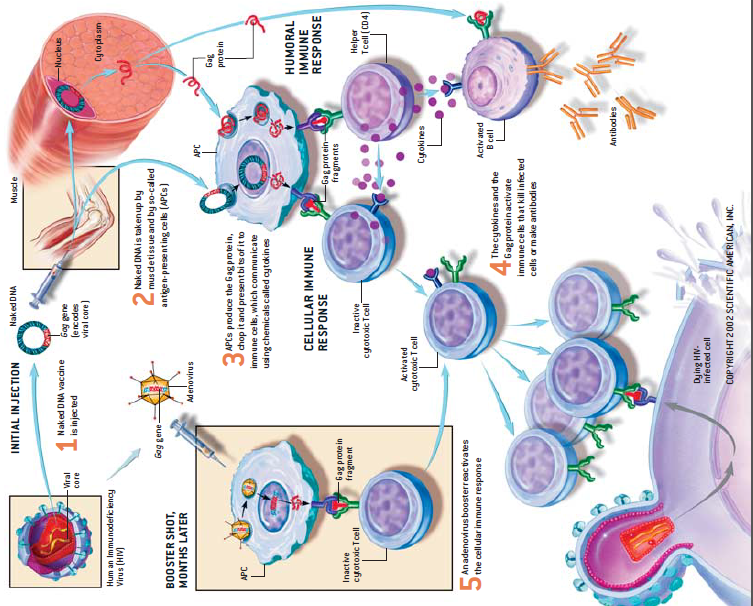
第二个试验是将连接在一起的HIV病毒的gag基因导入缺陷型的腺病毒中,这种病毒通常可以引起多种感冒。经过改变的腺病毒会将gag基因导入细胞,并且合成HIV的核心蛋白,同时诱导出对该蛋白的免疫反应。据Emini的报告,大约有44%到67%的志愿者接受腺病毒疫苗注射后,可以产生细胞免疫反应,反应强度因注射剂量和注射时间的长短而不同。
默克公司正在对DNA疫苗和腺病毒疫苗的联合使用效果进行试验,因为Emini预测这种复合疫苗效果可能是最好的。他说:“这个想法并不在于DNA疫苗本身是否是好疫苗,而是DNA疫苗是免疫系统的基础。”在DNA疫苗使用几个月以后,再注射腺病毒疫苗。然而可能出现的问题是,大多数人曾患腺病毒性感冒,因此这些人的免疫系统中存在清除腺病毒的“兵工厂”,在腺病毒疫苗给体细胞传输HIV基因并刺激艾滋病抗体之前,腺病毒就可能被消灭了。不过,增加腺病毒的剂量可能会克服这个问题。
Emini表示,由于针对体液免疫而研制的疫苗效果不佳,他和同事们将把重点放在细胞免疫上。他补充说:“抗体一直是个问题,从HIV感染者身上可以分离出许多种强有力的抗体,但是我们不知道如何通过疫苗产生这些抗体。
西雅图的Fred Hutchinson癌症研究中心的Lawrence Corey认为:“两者(体液免疫和细胞免疫)兼而有之是再好不过了,但最大的进展还是如何诱导细胞免疫反应。”Lawrence Corey也是国家资助的HIV疫苗试验网络的主要观察员。
抗体也是十分重要的,因为它们不但是免疫系统的第一道防线,也是防止病毒与细胞接触的关键。Corey说,针对激发细胞免疫而设计的疫苗(就像默克公司的疫苗)不容易防止感染,但是会使受感染者在同HIV病毒的斗争中保持一定的优势。Corey预测:“有抗体的患者HIV的潜伏期不只有8年,也许25年之后才有可能发作。”但是他补充道,还不能确定延缓疾病进程的疫苗是否会阻止艾滋病的流行,因为尽管HIV病毒在血液中含量很少,但是感染上病毒的患者仍然可以将其传染给别人。
由于其他的原因,诱导产生具有中和HIV能力的抗体是非常困难的。原因之一就是HIV通过改变自身的外型,使其在免疫系统做出反应之前就先行一步。与其他人类病毒不同的是,HIV变异频率非常快。Essex说:“当患者体内产生具有中和HIV的抗体时,它只能抵抗人体内1个月前的HIV病毒。”
许多科学家认为,只在理论上有效的分子——gp120(病毒用于侵袭免疫细胞的蛋白)构成的疫苗并不起作用,原因可能是这种疫苗的抗体结合到了该分子的错误部位。gpl20将其束缚在CD4(是gpl20进入到免疫细胞的第一步)表层的精确位置遮蔽起来,直到最后一刻,它才像弹簧刀一样地弹开。美国蒙大拿大学的Jack H.Nunberg和同事3年前曾在《Science》上发表论文指出,只要疫苗中的gpl20分子预先暴露给CD4,这样gP120的登陆位置就会暴露出来。但Corey认为:“要复制这种分子是很困难的。”研究人员对这种方法的前景持悲观态度。
艾滋病疫苗难以产生有效的HIV抗体的另一个原因是,HIV亚类病毒(subtype)的变异,这些变异在世界上不同的地方都产生了影响。HIV病毒主要有五种亚型,分别由A-F表示(见59页插图)。B型主要流行于北美和欧洲;非洲撒哈拉地区周围(也是全球艾滋病最为严重的地区)主要是C型;南亚及东南亚是艾滋病的第二大流行区,主要是B、C、E型。
一些研究表明,能识别某一亚型的抗体有可能识别不了其他亚型。也就是说,针对美国患者研制的艾滋病疫苗可能不适用于南非的患者。但是科学家对亚型间差异的重要性这个观点也各持己见,不同意只有与特定地区流行的某类亚型病毒相关的一类患者才能在该地区进行试验的说法。今年年底,Essex准备在博兹瓦那进行C型疫苗的第一阶段试验。他说,除非研究人员确定针对某种亚型的疫苗会与其他亚型的病毒发生交叉反应,否则他们坚持使用针对流行的病毒类型所研制的疫苗进行试验。交叉反应是在理想状态下发生的。但是他认为,除非我们已经知道,否则使用具体的亚型疫苗是非常重要的。
利用有交叉反应的亚型也避免出现发展中国家用人作为试验对象,来检测针对欧美各地研制的疫苗是否有效的现象。VaxGen公司在泰国试验的是B型和E型病毒的混合体。今年4月A型病毒在肯尼亚流行(A型病毒在此发现),国际艾滋病疫苗倡议组织(IAVI)因此而扩大了A型病毒疫苗试验范围。
但是今年1月,南非医学研究委员会的MalegaPuru william Makgoba和Nandipha Solomon以及南非艾滋病疫苗倡议组织的Timothy Johan Paul Tucker在英国医学杂志上撰文说:“HIV各类亚型之间的关系尚未确定。”他们声称,HIV病毒不同的亚型不但具有重要的政治和国家意义,也会影响到重大的国际试验的功效。
默克公司疫苗试验的初步数据表明,类型的差异不会影响细胞免疫。在今年2月的逆转录病毒大会上,Emini的报告显示,13名接受B型疫苗注射的志愿者中,有l0名患者体内的杀伤性细胞可以在试验中与A型或是C型病毒的蛋白发生反应。在细胞免疫中,可能会发生重要的亚型交又反应,但是抗体就不会出现交叉反应。Corey同时表示,不同亚型间的变化对细胞免疫的影响非常小,因为大多数杀伤性TfW胞识别的部分HIV与各种亚型所含的部分HIV是完全相同的。
NIAID的Johnston推断,是否每种疫苗都能应对5种亚型病毒的难题最终会有答案。加州埃默里维尔的Chiron正在研制一种多型疫苗(multiclade vaccine),并已进入早期临床试验。然而,Johnston认为这种疫苗的杀伤力太强。她提出警告,来自一种亚型病毒的蛋白将会被识别,而来自其他类型的蛋白都会浪费掉。
Weill医学院的Moore表示,不论亚型类别问题的结果如何,他和同事们都会比几年前更有信心,相信可以研制出能够诱导产生杀伤性T细胞和抗体的艾滋病疫苗。他说:“这个问题不是无法解决,只是难度太大。”
[菅金龙/译赵辉/校]
参考文献
HIV Vaccìne Efforts Inch Forward. Brian Vastag in Journal of the American Medical Association ,Vol.286,No. 15,pages 1826-1828; October 17,2001
For an overview of AIDS vaccine reseach ,including the status of U.S.-funded ADIS c1inical trials ,visit www.niaid .nih.gov/daids/vaccine/default.htm
A global perspective on the AIDS pandemic and the need for a vaccine can be found at the International AIDS Vaccine Initiative Web site: www.iavi.org
Joint United Nations Program on HIV/AIDS: www.unaids.org
肯尼亚的志愿者正在接受疫苗注射,这是在该国进行的艾滋病疫苗研究的一部分。
请 登录 发表评论